Linea guida
Carenza di ferro
Ultima revisione: 07/2022 Ultima modifica: 05/2023
1. Definizione, epidemiologia, stadi
Definizione
- La carenza di ferro è definita come una riduzione del ferro corporeo totale, L'anemia da carenza di ferro si verifica quando la concentrazione di emoglobina scende al di sotto del valore normale specifico per età o sesso a causa della carenza di ferro, secondo l'OMS < 12 g/dl nelle donne e < 13 g/dl negli uomini.
Epidemiologia
- Circa l'80 % di tutte le anemie sono anemie da carenza di ferro, l'80 % delle quali colpisce le donne (mestruazioni, gravidanze)
- Studi condotti in Europa e gli Stati Uniti: il 15–20 % di tutte le donne in età mestruale presenta una carenza di ferro senza anemia (soglia di ferritina: < 15 ng/ml), circa il 3 % presenta un'anemia manifesta da carenza di ferro (1, 2). La carenza di ferro è più comune nelle donne incinte che nelle donne non incinte
- Studio sullo stato del ferro in giovani donne (ZH): 22,7 % di carenza di ferro (soglia di ferritina: < 15 ng/ml), 2,2 % di anemia da carenza di ferro (4).
Stadi della carenza di ferro
A seconda della gravità, si distinguono 3 fase (5, 6)
Stadio 1: carenza di ferro non anemica
- Hb e MCV normale, ferritina ridotta; senza effetto sull'ematopoiesi.
Stadio 2: Eritropoiesi ferro-deficitaria
- Hb normale, ferritina ridotta (i valori limite variano), ematopoiesi e processi metabolici ferro-dipendenti possono essere compromessi a seconda delle comorbidità.
Stadio 3: Anemia da carenza di ferro (anemia ipocromica, microcitica)
- Hb < 12 g/dl (donne) o < 13 g/dl (uomini), MCV, MCH e conta eritrocitaria ridotta.
Nota: spesso l'Hb diminuisce più rapidamente della conta eritrocitaria. Anche se l'Hb è significativamente più bassa, la conta eritrocitaria può essere ancora nell'intervallo inferiore di normalità.
2. Cause e sintomi
Cause
La carenza di ferro è per lo più causata da una maggiore perdita di ferro o da un aumentato fabbisogno di ferro, meno spesso da disturbi dell'assorbimento. Le possibili cause sono illustrate nella tabella 1.
Tabella 1: cause dell'anemia da carenza di ferro
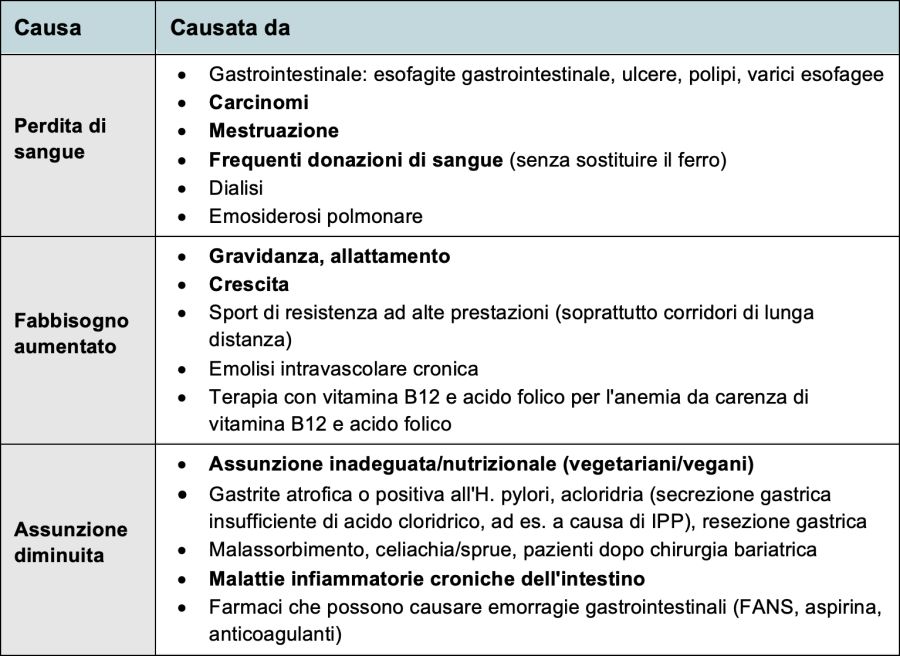
Nota: sono evidenziate le cause più importanti/comuni.
Sintomi
La comparsa dei sintomi dipende dalla durata e dalla gravità della carenza di ferro.
- Segni generali (a seconda della gravità e della durata)
- Debolezza muscolare e resistenza ridotta, affaticamento, irritabilità, vertigini
- Disturbi cognitivi (scarsa concentrazione, ridotta capacità di apprendimento, disturbi della memoria)
- Mal di testa, dispnea da sforzo, tachicardia, termoregolazione ridotta, appetito per argilla e terra.
- Pelle e mucose
- Pallore (segno incerto) della pelle e delle mucose (soprattutto congiuntive, segno più affidabile)
- Scanalature delle unghie, unghie fragili, perdita di capelli, pelle secca, prurito, afte, ragadi agli angoli della bocca.
Note su stanchezza e anemia
- Non esiste una relazione tra la fatica „isolata" e l'anemia in tutta la popolazione (8–10). D'altra parte, la fatica può essere alleviata/risolta dalla terapia del ferro nelle donne in premenopausa con carenza di ferro senza anemia (11) – ma in modo significativo solo nel caso di ferritina < 15 ng/ml (11, 12). Per il trattamento della carenza di ferro senza anemia, vedere il cap. 4.2.
- Se la stanchezza prima della terapia con ferro è inspiegabile, pensare anche ad altre malattie scatenanti, ad es. depressione, ipo/ipertiroidismo, insufficienza renale, diabete mellito, iperparatiroidismo, epatite cronica, ecc. (13). Vedi anche mediX GL Fatigue.
3. Diagnosi
3.1. Diagnosi di laboratorio
Sono necessari i seguenti parametri: ematogramma, ferritina sierica, PCR (15).
Anemia da carenza di ferro
- Hb < 12 g/dl (donne), < 13 g/dl (uomini); anemia lieve: Hb 9–12 g/dl, anemia grave: 6–7 g/dl
- Ferritina (valori soglia in parte contestati)
- < 15 ng/ml: indica riserva di ferro esaurita
- 15–30 ng/ml: carenza di ferro con riserva di ferro ridotta
- 30–50 ng/ml: riserva di ferro sufficiente se non è presente un'infiammazione concomitante
⇒ Si può assumere una carenza di ferro quando la ferritina sierica è < 15 ng/ml, con sintomi corrispondenti (15, 20, 21). Nei pazienti con alcune malattie croniche si applicano valori soglia diversi (vedere sotto la sezione „Screening“)
- Nei pazienti ematologici e oncologici, la saturazione della transferrina può essere determinata in aggiunta alla ferritina (spesso risultano valori elevati „infiammatori“). La saturazione della transferrina ridotta significa che non c'è abbastanza ferro disponibile per l'eritropoiesi. Questo può avvenire in caso di valori di infiammazione aumentati, anche se le riserve di ferro sono ben riempite.
⇒ Una saturazione della transferrina ≤ 20 % è considerata diagnostica di carenza di ferro, anche in caso di neoplasia, insufficienza cardiaca e insufficienza renale cronica (15, 22).
Nota: il ferro sierico è obsoleto come parametro diagnostico di carenza di ferro.
Diagnosi differenziale
Un'anemia ipocromica microcitica può essere presente anche in forme lievi di anemia ereditaria come l'alfa- o la beta-talassemia o in malattie croniche.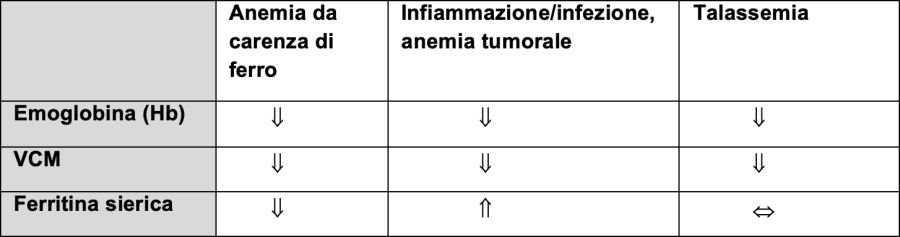
Nota: le anemie da infiammazioni, da infezioni e da tumori sono spesso normocromiche, la carenza di ferro in combinazione con la carenza di vitamina B12 può essere normocitica!
3.2. Chiarimento delle cause
La carenza di ferro (l'anemia da carenza di ferro) è solo un sintomo e la sua eziologia deve essere prima chiarita.
- Alimentazione (vegetariano/vegano)?
- Donatore di sangue?
- Ipermenorrea?
- Assunzione di Aspirina®, FANS, Marcoumar® (emorragia gastrointestinale cronica)?
- Sprue oligosintomatica con sintomi gastrointestinali (perdita di peso, diarrea, dolore addominale)? –> chiarire con le IgA transglutaminasi tissuali e le IgA totali.
In assenza di chiare indicazioni anamnestiche, le malattie infiammatorie maligne e croniche del tratto gastrointestinale devono essere escluse in via prioritaria. Se non c'è un sospetto concreto, si deve procedere a un chiarimento in base all'età
- Pazienti < 50 anni: prima gastroscopia con biopsia dell'intestino tenue (dubbio di sprue), se non ci sono risultati –> colonscopia
- Pazienti > 50 anni: prima sensore OC o colonscopia, se non ci sono risultati –> gastroscopia.
Screening
- Lo screening generale per la carenza di ferro senza sintomi corrispondenti non è raccomandato
- I pazienti con insufficienza cardiaca spesso presentano un'anemia concomitante (circa il 55 % nell'insufficienza cardiaca cronica). I pazienti con insufficienza cardiaca spesso presentano un'anemia concomitante. Questi pazienti dovrebbero quindi essere sottoposti a uno screening annuale per l'anemia da carenza di ferro. Secondo la linea ESC Guideline 2021, una carenza di ferro è presente con una ferritina sierica < 100 ng/ml, ma questa soglia è controversa
- I pazienti con anemia infiammatoria cronica (eritrociti ipo- a normocromici, saturazione della transferrina < 20 %, parametri infiammatori [+]), ad es. malattie infiammatorie croniche dell'intestino, dovrebbero essere sottoposti a screening regolari per la carenza di ferro (non esistono raccomandazioni generali esatti sugli intervalli di screening). Se la ferritina sierica è < 30 ng/ml, si deve presumere una carenza assoluta di ferro che richiede una terapia
- Nell'insufficienza renale cronica, la carenza di ferro deve essere controllata periodicamente secondo le raccomandazioni (28). Nei pazienti senza anemia e eTIG≥ 45 ml/min/1,73 m2 ogni anno, in caso di eTIG < 45 ml/min/1,73 m2 almeno 2 volte l'anno. Nei pazienti con anemia (ma senza farmaci stimolanti per l'eritropoietina): in caso di anemia lieve e eTIG ≥ 45–60 ml/min/1,73 m2 ogni 6 mesi, in caso di malattia rapidamente progressiva, anemia grave e eTIG < 45 ml/min/1,73 m2 ogni 3 mesi. Le soglie di ferro in base al grado di insufficienza renale sono controverse.
4. Terapia
4.1. Alimentazione
L'apporto di ferro può essere aumentato con una dieta ricca di ferro e quindi è possibile prevenire la carenza di ferro. Nel caso di una carenza di ferro già esistente, di solito è necessario un'ulteriore sostituzione con farmaci.
- Fabbisogno di ferro
- Assunzione con gli alimenti al giorno

- Alimentazione
- Circa il 40–90 % del ferro animale è presente come ferro eme divalente facilmente assorbibile (mioglobina, emoglobina, citocromi) che può essere assorbito moto più efficacemente attraverso il proprio trasportatore rispetto al ferro non eme di altri alimenti. Il „ferro vegetale“ è presente in forma trivalente e può essere assorbito solo dopo la riduzione a Fe2+
- Il Fe3+ non è assorbibile a un pH > 3. Ha bisogno dell'acido gastrico e/o acido ascorbico (attenzione in caso di terapia con IPP)
- Il ferro non eme (ferro libero) può essere promosso o inibito nel riassorbimento.
- Il riassorbimento è favorita da
- Alimenti fermentati (pH basso), ad es. i crauti
- Acidi organici (agrumi e altri frutti, succhi di frutta ai pasti).
Nota: contrariamente a quanto ipotizzato in precedenza, la vitamina C non sembra avere un'influenza significativa sul riassorbimento del ferro (24).
- l riassorbimento è inibito da
- Fitati: ad es. la crusca (sostanza contenuta nel guscio esterno del grano. Lega diversi nutrienti nell'intestino, come ferro, zinco, calcio o magnesio, che vengono poi espulsi non digeriti)
- Ossalato (spinaci)
- Composti polifenolici (tè nero, caffè, tisane, cacao, vino rosso, origano)
- Calcio (latte): diverse informazioni sul signifcato dell'inibizione dell'assorbimento del ferro.
- Buone fonti di ferro sono (tabella completa sul contenuto di ferro agli alimenti in iron.medline)
- Carne (la carne rossa ha la maggior quantità di ferro utilizzabile), fegato
- Legumi (soia, lenticchie, ceci)
- Noci e semi (pistacchi, mandorle, nocciole, semi di girasole, semi di lino)
- Cereali (soprattutto integrali)
- Verdure e erbe (prezzemolo, crescione, tarassaco, cipolle, salsefrica)
- Le pentole in ghisa aumentano il contenuto di ferro negli alimenti.
- Il riassorbimento è favorita da
- Assunzione con gli alimenti al giorno
4.2. Sostituzione del ferro
Indicazione
- Ogni anemia da carenza di ferro è un'indicazione per la sostituzione del ferro
- Uno studio controllato con placebo (2020) su donatori di sangue con carenza di ferro, ma senza anemia, ha rilevato che l'integrazione di ferro per via endovenosa non influisce sull'affaticamento o su altri sintomi come qualità di vita diminuita, riduzione del rendimento lavorativo, deterioramento cognitivo, sbalzi d'umore e „gambe senza riposo“ (20). E quindi discutibile se la carenza di ferro senza anemia debba essere tratta.
- Nella carenza di ferro senza anemia e valori iniziali di ferritina > 15 ng/ml, la sostituzione del ferro non è indicata (5, 6, 15, 16, 20) perché il suo benefico non è sufficientemente dimostrato. Questo vale anche per i pazienti con sindrome delle gambe senza riposo (14, 20) –> vedi anche mediX GL Disturbi del sonno (cap.5)
- Nella carenza di ferro senza anemia e valori di ferritina < 15 ng/ml, si può considerare la sostituzione del ferro, anche se il beneficio è discutibile
- La sostituzione del ferro in presenza di riserve di ferro piene (e ferritina normale) non è indicata ed è potenzialmente dannosa (6, 25).
La sostituzione del ferro nel caso di comorbidità
- Insufficienza cardiaca: nei pazienti sintomatici con FEVS < 45 % e carenza di ferro (definita come ferritina sierica < 100 ng/ml), la linea guida 2021 della ESC raccomanda la terapia con ferro per via endovenosa con carbossimaltoso ferrico (Ferinject®). Lo studio AFFIRM-HF (2020) ha rilevato che la terapia con ferro riduce il rischio di ospedalizzazione in questi pazienti. Tuttavia, l'endpoint primario dello studio - la combinazione di morte cardiovascolare e riospedalizzazione per insufficienza cardiaca - non ha raggiunta la significatività statistica. Vedi anche mediX GL Insufficienza cardiaca (cap. 4, sezione Sostituzione del ferro)
- Malattie infiammatorie croniche intestinali (MICI): il ferro dovrebbero essere sostituito nei pazienti con MICI con anemia infiammatoria e livelli di ferritina sierica < 30 μg/l (27). Il beneficio della terapia con ferro nei pazienti con MICI con carenza di ferro ma senza anemia è controverso e non ancora stato stabilito (–> Linea guida/consenso ECCO)
Se è necessaria una terapia: sono possibili terapie con ferro per via orale o endovenosa, la decisione viene presa individualmente. La terapia con ferro per via endovenosa è utile nei casi di reazione infiammatoria acuta pronunciata, di aumento inadeguato dell'Hb con la terapia orale e nei casi di bassi valori di Hb quando un'aumento rapido dell'Hb è desiderato (–> Universimed) - Anemia renale –> vedi mediX GL Insufficienza renale cronica (cap. 3.5). I valori soglia per la terapia sono controversi
- Donne incinte: valore soglia dell'Hb inferiore < 11 g/dl (nel 2° trimestre < 10,5 g/dl); ferritina siercia < 30 ng/ml in gravidanza è un'indicazione per il trattamento, anche in assenza (attuale) di anemia (19). Giustificazione: fabbisogno cresciuto di ferro nella gravidanza, perdita di sangue prevista durante il parto e fabbisogno cresciuto durante l'allattamento.
Dosaggio e applicazione

Regola generale per la dose di ferro in base al valore iniziale della ferritina (5):
Ferritina sierica
- < 10 ng/ml –> dose totale di 1'000 mg di ferro
- 10–30 ng/ml –> dose totale cumulativa di 500 mg di ferro
- 30–50 ng/ml –> dose di 200 mg di ferro.
Nota: se è presente un'anemia da carenza di ferro, è necessario calcolare il fabbisogno di ferro, altrimenti basta seguire la regola generale.
1. La sostituzione del ferro per via orale continua ad essere la somministrazione standard.
Dosaggio
- Negli adulti 100–150 mg a giorni alterni (migliore assorbimento del ferro rispetto all'assunzione quotidiana [17]). Assumere almeno 30 min prima del pasto (in pazienti sensibili allo stomaco durante/dopo aver mangiato, ma con un assorbimento leggermente inferiore)
- Nei pazienti molto anziani (≥ 80 J.), si può scegliere anche una dose bassa (16). In uno studio pertinente, una dose giornaliera di 15 mg di ferro si è rivelata efficace quanto le dosi comparativi di 50 mg e 150 mg, e significativamente più tollerabile (18)
- Nelle donne con desiderio di diventare incinta, si raccomanda un'ulteriore sostituzione con acido folico.
Farmaci
- Fe2+: Tardyferon®, Ferrum Hausmann®
- Fe3+: solo forma orale Maltofer® (leggermente meglio tollerato del Fe2+, ma assorbimento leggermente peggiore)
Effetti collaterali: gli effetti gastrici (nausea) o la costipazione limitano abbastanza spesso la terapia –> ridurre la dose di ferro, eventualmente passare alla forma in gocce per alleviare gli effetti collaterali.
Controindicazioni: anemie con livelli di ferritina normali, emosiderosi ed emocromatosi con livelli elevati di ferritina.
2. La sostituzione del ferro per via endovenosa può essere utile se il ferro orale non è tollerato o non è sufficientemente assorbito, così nelle donne incinte, nelle malattie infiammatorie croniche dell'intestino o nelle malattie renali chroniche (16)
- Con 100 mg di ferro, la ferritina può essere aumentata di circa 10 ng/ml. Somministrare imperativamente per via endovenosa (usare Venflon)!
- Somministrare Ferinject® (ferro carbossimaltoso) in infusione breve (diluito in soluzione salina fisiologica): 500–1'000 mg in 250 ml di NaCl 0,9 % e durata minima di infusione 15 minuti. Dosaggio: 20 mg di ferro/kgPC. Per la prima infusione di ferro non si devono superare i 500 mg. Se il paziente lo tollera bene e se il fabbisogno è elevato, si possono somministrare 1'000 mg alla volta nel corso del trattamento. In alternativa a Ferinject® si può somministrare Monofer® (ferro maltosoide) con efficacia e tollerabilità comparabili. Dosaggio Monofer®: dose massima giornaliera di 20 mg/kgPC (durata di infusione min. 15 min per le dosi fino a 1'000 mg, per le dosi > 1'000 mg la durata di infusione è di 30 min o più)
- Monofer® non richiede una dose di prova. Costo: leggermento più economico rispetto a Ferinject® (differenza di prezzo circa CHF 5.– o CHF 12.– per 500 mg 1'000 mg rispettivamente)
- La dose massima settimanale di 1'000 mg di ferro o 20 mg/kgPC non deve essere superata! Dettagli in: Scheda informativa Infusioni di ferro (esempio Ferinject®). Non esiste una limite di dose di 1'000 mg per Monofer®
- Infusioni di ferro in gravidanza: non prima del 2° trimestre.
Effetti collaterali
- Le reazioni anafilattiche gravi sono estremamente rare (< 1:1‘200‘000 dosi), ma massicce quando si verificano (26). Le reazioni non allergiche transitorie associate all'infusione comprendono sintomi di vampate, palpitazioni, malessere, vertigini, mialgie e febbre (nello 0,5–1 % delle infusioni). Ripetute infusioni di ferro possono portare a un sovraccarico di ferro e le complicazioni concomitanti
- Nei pazienti con insufficienza renale cronica trattati con agenti stimolanti l'eritropoesi, ulteriori infusioni di ferro devono essere evitate se la saturazione della transferrina è > 30 % o la ferritina > 500 ng/ml (23)
- Le infusioni di ferro possono essere seguite da ipofosfatemie per lo più passive, ma in singoli casi gravi (29–31).
Note:
L'ipofosfatemia è più frequente e più pronunciata con Ferinject che con Monofer. Tuttavia, la rilevanza clinica di questi risultati di laboratorio non è ancora chiara. In nessuno degli studi i risultati clinici rilevanti sono stati chiaramente correlati con il livello di fosfato misurato (30, 31).
⇒ mediX raccomanda
- Non misurare di routine il fosfato prima dell'infusione di ferro
- I pazienti che dopo l'infusione di ferro mostrano maggiore affaticamento e stanchezza generale rispetto a prima dell'infusione, o che manifestano problemi respiratori ed effetti collaterali gastrointestinali, possono indicare un'ipofosfatemia clinicamente rilevante. In questi casi si raccomanda di misurare il fosfato nel plasma
- Se è prevista un'altra infusione di ferro, mediX raccomanda di misurare preventivamente il fosfato per decidere quale preparato scegliere per l'infusione di ferro.
Procedura in caso di effetti collaterali
Misure di emergenza in caso di reazioni gravi (anafilattiche) (–> mediX Piano di emergenza)
Per reazioni meno gravi (senza ipotensione, tachicardia, tachipnea, stridore, edema periorbitale)
- Interrompere l'infusione e osservare il paziente (senza somministrare alcun farmaco)
- Se i sintomi si risolvono, continuare l'infusione (= decorso più comune)
- Se i sintomi peggiorano –> trattare come reazione grave
- Se i sintomi persistono, somministrare metilprednisone per via endovenosa, attendere 30 minuti e ricominciare l'infusione.
Cosa fare in caso di allergia al preparato per via endovenosa e fabbisogno di una nuova infusione di ferro?
⇒ Provare un'altro preparato (vedere anche la sezione „Preparati di ferro per via endovenosa“ in Universimed)
o
⇒ Pretrattamento con prednisolone e farmaci antiallergici sotto maggiore monitoraggio (preferibilmente in ospedale).
4.3. Controllo della terapia
⇒ Non c'è consento sulla durata della sostituzione del ferro
- In caso di carenza di ferro sintomatica non anemica, la durata della sostituzione può essere determinata in base alla ferritina e allo stato di salute
- In caso di carenza di ferro con anemica, anche le riserve di ferro devono essere reintegrate con la sostituzione del ferro (ferritina sierica: 50–100 ng/ml).
Controlli nell'anemia da carenza di ferro (6)
- Emoglobina dopo 4 settimane (dovrebbe essere aumentata di circa 2 g/dl)
- Ulteriori controlli dell'Hb: ogni 4 settimane fino alla normalizzazione del valore Hb
- Misurazione della ferritina: 6–8 settimane dopo l'ultima assunzione di ferro per controllare le riserve di ferro, in caso di terapia di ferro per via endovenosa dopo 12 settimane.
5. Bibliografia
- Looker AC, et al.: Iron deficiency – United States, 1999–2000. Morb Mortal Wkly Rep. 2002;51:897–99.
- Galan P, et al.: Determinig factors in the iron status of adult women in the SU.VI.MAX.study. Eur J Clin Nutr. 1998;52:383–8.
- Schleiffenbaum BE, et al.: Unexpected high prevalence of metabolic disorders and chronic disease among young male draftees – the Swiss Army XXI experience. Swiss Med Wkly 2006; 18: 175–184.
- Sempach JS: Ernährungsgewohnheiten und Nährstoffstatus von jungen Frauen in Zürich (Dietary patterns and nutrient intake in young women in Zürich). PhD thesis. Zurich: Swiss Federal Institute of Technology Zürich, 1995: 1–144.
- Clénin G, et al.: Consensus statement of the Swiss Society of Sports Medicine. Iron deficiency in sports – definition, influence on performance and therapy. Swiss Med Wkly. 2015;145:w1419 Swiss Medical Weekly, 2015.
- Clénin G: The treatment of iron deficiency without anaemia (in otherwise healthy persons). Swiss Med Wkly. 2017;147:w14434 Swiss Medical Weekly, 2017.
- Masche U.P: Eisentherapie. Pharma-kritik, Ausgabe 17/2006.
- Wood MM, Elwood PC: Symptoms of iron deficiency anaemia. A Community survey. Brit J Prev Soc Med 1966; 20: 117.
- Elwood PC, Waet, et al.: Symptoms and circulating haemoglobin level. J Chron Dis 1969; 21: 615-28.
- Knottnerus JA, Knipet, et al.: Unexplained Fatigue and Hemoglobin: A Primary Care Study. Can Fam Physican 1986; 32: 1601-4.
- Krayenbühl P-A, Battegay E, et al.: Intravenous iron for the treatment of fatigue in nonanemic, premenopausal women with low serum ferritin concentration. Blood. 2011;118(12):3222-3227.
- Von Drygalski A, Adamson JW: Ironing out fatigue. Blood 2011;118(12):3191–2.
- Martius F: Eisenmangel ohne Anämie. Nicht hämatologische Auswirkungen des Eisenmangels: Welche sind belegt, wann kommen sie zum Tragen? Schweiz Med Forum 2009; 9(15-16):294-299.
- Trotti LM, Bhadriraju S, Becker LA: Iron for restless legs syndrome. Cochrane Database of Systematic Reviews 2019, https://doi.org/10.1002/14651858.CD007834.pub3.
- Schrier SL: Causes and diagnosis of iron deficiency and iron deficiency anemia in adults. UpToDate, aufgerufen 06/2022.
- Schrier SL, Auerbach M: Treatment of iron deficiency anemia in adults UpToDate, aufgerufen 06/2022.
- Stoffel NU, et al.: Iron absorption from oral iron supplements given on consecutive versus alternate days and as single morning doses versus twice-daily split dosing in iron-depleted women: two open-label, randomised controlled trials. Lancet Haematol. 2017;4(11):e524. Epub 2017 Oct 9.
- Rimon E, et al.: Are we giving too much iron? Low-dose iron therapy is effective in octogenarians. Am J Med.2005 Oct;118(10):1142-7.
- Schweizerische Gesellschaft für Gynäkologie und Geburtshilfe (SGGG): Diagnostik und Therapie der Eisenmangelanämie in der Schwangerschaft und postpartal. SGGG, 1/2017.
- Keller P, et al.: The effects of intravenous iron supplementation on fatigue and general health in non-anemic blood donors with iron deficiency: a randomized placebo-controlled superiority trial. Sci Rep 10, 14219 (2020). https://doi.org/10.1038/s41598-020-71048-0.
- Garcia-Casal MN, et al.: Serum and plasma ferritin as an index of iron deficiency and overload. Cochrane Database of Systemic Reviews 2021, Issue 5.
- Gattermann N, Muckenthaler M, Kulozik AE, Metzgeroth G, Hastka J: The evaluation of iron deficiency and iron overload. Dtsch Arztebl Int 2021; 118: 847–56. DOI: 10.3238/arztebl.m2021.0290.
- Tichelli A: Gegenwärtiger Stand der intravenösen Eisentherapie. Sept. 2019.
- Li N, et al.: The Efficacy and Safety of Vitamin C for Iron Supplementation in Adult Patients With Iron Deficiency Anemia: A Randomized Clinical Trial. JAMA Netw Open. 2020;3(11):e2023644. Epub 2020 Nov 2.
- Shah AA, et al.: Risk of Infection Associated With Administration of Intravenous IronA Systematic Review and Meta-analysis. JAMA Netw Open. 2021;4(11):e21sued33935.
- Dave CV, et al.: Risks for anaphylaxis with intravenous iron formulations. A retrospective cohort study. Ann Intern Med. 29 March 2022 https://doi.org/10.7326/M21-4009.
- Resál T, Farkas K and Molnár T (2021): Iron Deficiency Anemia in Inflammatory Bowel Disease: What Do We Know? Front. Med. 8:686778.
- Berns JS: Treatment of anemia in nondialysis chronic kidney disease. UpToDate, aufgerufen 06/2022.
- Schaefer B, Tobiasch M, Viveiros A, et al.: Hypophosphataemia after treatment of iron deficiency with intravenous ferric carboxymaltose or iron isomaltoside—a systematic review and meta-analysis. Br J Clin Pharmacol. 2021; 87: 2256–2273. https://doi.org/10.1111/bcp.14643.
- Fragkos KC, Sehgal V, Rogers J, et al.: Hypophosphataemia after intravenous iron therapy with ferric carboxymaltose—Real world experience from a tertiary centre in the UK. GastroHep. 2020; 2: 205– 214. https://doi.org/10.1002/ygh2.415.
- Zoller H, Wolf M, et al.: Hypophosphataemia following ferric derisomaltose and ferric carboxymaltose in patients with iron deficiency anaemia due to inflammatory bowel disease (PHOSPHARE-IBD): a randomised clinical trial. Gut. 2023 Apr;72(4):644-653. doi: 10.1136/gutjnl-2022-327897. Epub 2022 Sep 9. PMID: 36343979; PMCID: PMC10086283.
6. Informazioni legali
Questa linea guida è stata aggiornata nel luglio 2022. Ultima modificazione: maggio 2023
© Associazione mediX schweiz
Editrice
Prof. Dr. med. Corinne Chmiel
Redazione
Prof. Dr. med. Corinne Chmiel
Dr. med. Uwe Beise
Dr. med. Felix Huber
Dr. med. Maria Huber
Autori
Prof. Dr. med. Corinne Chmiel
Dr. med. Uwe Beise
Questa linea guida è stata preparata senza influenze esterne con la collaborazione di tutte le reti mediche regionali mediX e delle reti mediche associate in Svizzera. Non vi sono dipendenze finanziarie o di contenuto dall'industria o da altre istituzioni o gruppi di interesse.
Le linee guida mediX contengono raccomandazioni terapeutiche per specifici disturbi o situazioni di trattamento. Tuttavia, ogni paziente deve essere trattato in base alla sua situazione individuale.
Sebbene le linee guida mediX siano sviluppate e controllate con grande cura, l’associazione mediX schweiz non può assumersi alcuna responsabilità per la loro correttezza, in particolare per quanto riguarda le informazioni sul dosaggio.
Tutte le linee guida mediX su Internet al indirizzo www.medix.ch
L’associazione mediX schweiz è un’associazione di reti di medici e di medici in Svizzera.
Associazione mediX schweiz, Sumatrastr.10, 8006 Zurigo
Si prega di inviare un feedback a: